Лекция № 15. Биологически активные гетероциклические соединения
Лекция № 15
Биологически активные гетероциклические
соединения
План
- Классификация.
- Пятичленные азотсодержащие гетероциклы с
одним гетероатомом. - Шестичленные азотсодержащие гетероциклы с
одним гетероатомами. - Пяти- и шестичленные гетероциклы с двумя
атомами азота.
Лекция № 15
Биологически активные гетероциклические
соединения
План
- Классификация.
- Пятичленные азотсодержащие гетероциклы с
одним гетероатомом. - Шестичленные азотсодержащие гетероциклы с
одним гетероатомами. - Пяти- и шестичленные гетероциклы с двумя
атомами азота.
Гетероциклическими называют соединения, молекулы
которых содержат циклы, включающие наряду с атомами углерода один или несколько
гетероатомов. Гетероциклы – самый многочисленный класс органических соединений,
включающий около 2/3 всех известных природных и синтетических органических
веществ. К гетероциклам относятся многие алкалоиды, витамины, природные
пигменты. Они являются структурными фрагментами молекул нуклеиновых кислот и
белков. Более 60% наиболее известных и широко употребляемых лекарственных
препаратов являются гетероциклическими соединениями.
1. Классификация
Гетероциклы классифицируют по следующим основным признакам:
- по природе и числу гетероатомов;
- по размеру цикла;
- по степени ненасыщенности.
Наибольшее распространение в
природе имеют пяти- и шестичленные гетероциклы, содержащие в качестве
гетероатомов азот, а также кислород и серу.
По степени ненасыщенности различают насыщенные, ненасыщенные и ароматические
гетероциклы. Гетероциклы неароматического характера по своим свойствам сходны с
соответствующими ациклическими соединениями (аминами, амидами, простыми и
сложными эфирами и т.д.). 5- и 6-членные гетероциклы, замкнутая сопряженная
система которых включает (4n + 2) электрона, обладают ароматическим характером
(см. лек. №2). Такие соединения по свойствам родственны бензолу и относятся к
ароматическим гетероциклическим соединениям. Для них, как и для бензоидных
систем, наиболее характерны реакции замещения. При этом гетероатом выполняет
роль “внутренней” функции, определяющей скорость и направление реакций
замещения.
Именно ароматические гетероциклические соединения широко распространены в
природе. Далее будут рассмотрены азотсодержащие ароматические гетероциклы.
2. Пятичленные азотсодержащие гетероциклы с одним
гетероатомом
Пиррол
Пиррол – 5-членный ароматический гетероцикл с одним атомом азота.
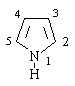
Ароматическая система пиррола включает 6 p -электронов:
четыре p -электрона от двойных связей и два – от гетероатома.
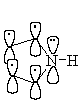
Атом азота с неподеленной парой электронов
действует как донор, повышая электронную плотность на атомах углерода цикла.
Поэтому пиррол относят к p -избыточным гетероциклам.
Химические свойства
Химические свойства пиррола определяются наличием ароматической системы и
полярной связи N-H.
Кислотно-основные свойства
Неподеленная пара электронов азота является частью ароматического секстета
электронов, поэтому пиррол практически лишен основных свойств (![]() ). Сила пиррола как основания не может
). Сила пиррола как основания не может
быть точно определена, так как он является ацидофобным соединением и
полимеризуется под действием кислот.
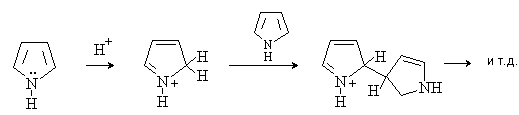
В то же время, наличие полярной связи N-H
обуславливает слабые кислотные свойства пиррола (pKa=16,5).
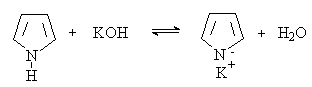
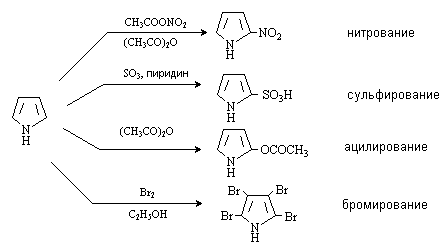
Реакции электрофильного
замещения
Пиррол, как p -избыточный гетероцикл, легко вступает в реакции электрофильного замещения.
Активность пиррола по отношению к электрофилам выше, чем у бензола, и близка к
активности анилина и фенола. Электрофильное замещение направляется
преимущественно в положение 2. Из-за ацидофобности пиррола
SE-реакции проводятся в
отсутствии кислот.
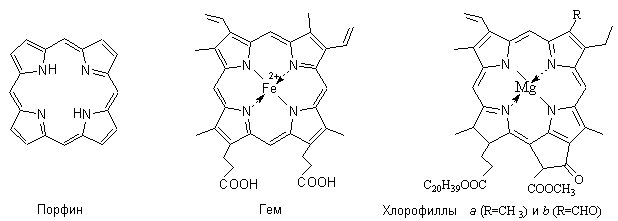
Биологически активные производные
пиррола.
Тетрапиррольные соединения содержат ароматический макроцикл порфин, включающий четыре пиррольных кольца.
Замещенные порфины называют порфиринами. В виде комплексов с
металлами порфирины и частично гидрированные порфирины входят в состав важных
природных соединений – гема (простетической группы гемоглобина –
содержащегося в эритроцитах основного белка дыхательного цикла, переносчика
кислорода от органов дыхания к тканям), зеленого пигмента растений хлорофилла, витамина В12.
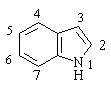
Индол
Индол – ароматическое гетероциклическое соединение, содержащее
конденсированные бензольный и пиррольный циклы.
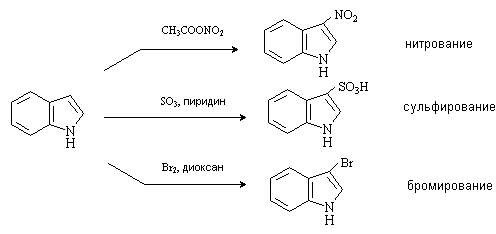
Химические свойства
Химические свойства индола аналогичны свойствам пиррола. Он практически не
обладает основными свойствами, ацидофобен, является слабой NH-кислотой.
Активно вступает в реакции электрофильного замещения, при этом заместитель
вступает в положение 3 пиррольного кольца.
Биологически активные производные
индола.
Триптофан – незаменимая (не
синтезируется в организме человека) аминокислота, входящая в состав животных и
растительных белков.
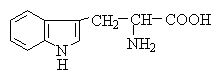
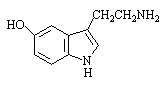
Серотонин – биогенный амин,
продукт метаболизма триптофана. Обладает высокой биологической активностью,
является нейромедиатором головного мозга.
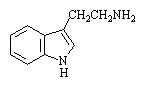
Триптамин – токсичный биогенный
амин, продукт декарбоксилирования триптофана.
Индольные алкалоиды. Алкалоиды –
гетероциклические азотсодержащие основания растительного происхождения,
обладающие ярко выраженным физиологическим действием. Индольное кольцо входит
в состав многих алкалоидов – резерпина (содержится в растениях рода
раувольфия; используется как успокаивающее и понижающее кровяное давление
средство), стрихнина (содержится в семенах растения чилибухи; используется как
тонизирующее средство), лизергиновой кислоты (алкалоид спорыньи; диэтиламид
лизергиновой кислоты — ЛСД — сильное галлюциногенное средство).
3. Шестичленные азотсодержащие гетероциклы с одним
гетероатомами.
Пиридин
Пиридин – 6-членный ароматический гетероцикл с одним атомом азота.
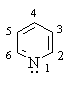
Ароматическая система пиридина включает 6 p -электронов и
подобна ароматической системе бензола: каждый атом цикла подает в ароматический
секстет один р-электрон. Неподеленная пара электронов азота в силу своей
пространственной ориентации в сопряжении не участвует
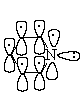
Атом азота действует как акцептор, понижая
электронную плотность на атомах углерода цикла. Поэтому пиридин относят к p -дефицитным гетероциклам.
Химические свойства
Химические свойства пиридина определяются наличием ароматической системы и
основного атома азота.
Основные и нуклеофильные свойства.
Пиридин проявляет слабые основные свойства (![]() =5,23) за счет неподеленной пары электронов
=5,23) за счет неподеленной пары электронов
азота и с кислотами образует соли пиридиния.
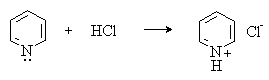
Атом азота пиридина проявляет также
нуклеофильные свойства и алкилируется алкилгалогенидами с образованием солей
алкилпиридиния.
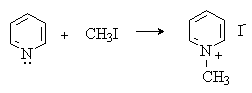
Соли алкилпиридиния легко взаимодействуют с
нуклеофильными реагентами, в том числе с комплексными гидридами металлов
(NaBH4), с образованием продуктов
присоединения. Подобные процессы лежат в основе механизма действия кофермента
НАД+ (см. лек. № 19).
Реакции электрофильного замещения
Реакции электрофильного замещения для пиридина
идут с большим трудом, что обусловлено p -дефицитностью ядра и способностью атома азота
образовывать соли с протонными кислотами и комплексы с кислотами Льюиса, что еще
больше уменьшает нуклеофильность ядра. По способности к электрофильному
замещению пиридин напоминает нитробензол. Атака электрофилами идет по положению
3.
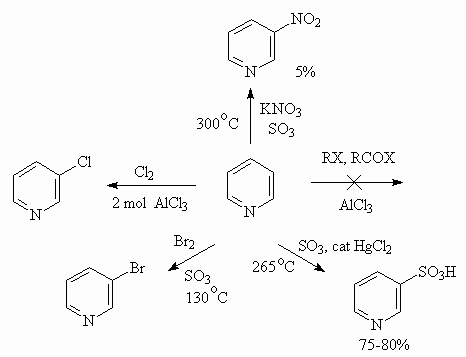
Реакции нуклеофильного замещения
Наиболее характерными для пиридина являются реакции нуклеофильного замещения,
которые идут по положениям 2 и 4. Примерами таких реакций является
взаимодействие пиридина с амидом натрия (реакция Чичибабаина) и со щелочами.
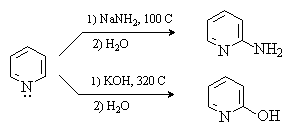
Окисление и восстановление
Цикл пиридина устойчив к действию окислителей. Алкилпиридины окисляются с
образованием пиридинкарбоновых кислот.
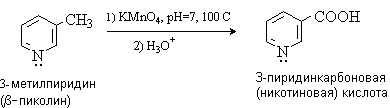
Пиридин гидрируется в жестких условиях с
образованием насыщенного гетероцикла – пиперидина.
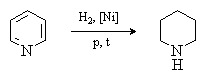
Соли алкилпиридиния легко восстанавливаются
комплесными гидридами металлов (см. выше).
Биологически активные производные
пиридина.
Никотиновая кислота (см. выше) и
ее амид — никотинамид — две формы витамина РР. Никотинамид является
составной частью ферментативных систем, ответственных за
окислительно-восстановительные процессы в организме. Диэтиламид никотиновой
кислоты – кордиамин – эффективный стимулятор центральной нервной
системы.
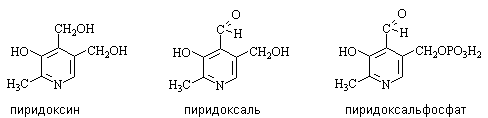
Пиридоксин и пиридоксаль – различные
формы витамина В6,
предшественники кофермента пиридоксальфосфата, участвующего в процессах
синтеза аминокислот из кетокислот путем трансаминирования (см. лек. №16).
Никотинамиадениндинуклеотид – кофермент, участвующий в процессах окисления и восстановления, связанных с
переносом гидрид-аниона (см. лек. №19).
Пиридиновые алкалоиды. Ядро пиридина и пиперидина входит в состав
многих алкалоидов – никотина и анабазина (алкалоиды, содержащиеся в листьях
табака; чрезвычайно токсичны, используются как инсектициды), атропина
(содержится в растениях семейства пасленовых; высокотоксичен; применяется в
медицине как средство, вызывающие расширение зрачка), кокаина (содержится в
листьях коки; стимулирует и возбуждает нервную систему, известен как одно из
первых местноанестезирующих и наркотических средств).
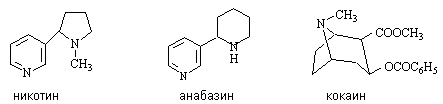
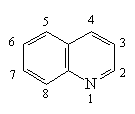
Хинолин и
изохинолин
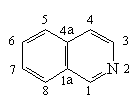
Хинолин и изохинолин – ароматические гетероциклические соединения, содержащие
конденсированные бензольный и пиридиниевый циклы.
 |
 |
хинолин |
изохинолин |
Химические свойства
Химические свойства хинолина и изохинолина аналогичны свойствам пиридина. Они
обладают основными и нуклеофильными свойствами и образуют соли при
протонировании сильными кислотами и при алкилировании алкилгалогенидами. Реакции
электрофильного замещения протекают по наименее электронодефицитному бензольному
кольцу и направляются в хинолине в положения 6 и 8. Нуклеофильные реагенты
атакуют пиридиниевый цикл хинолина в положение 2.
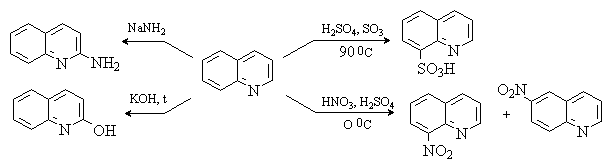
При каталитическом гидрировании хинолина в
первую очередь затрагивается пиридиниевый цикл. При окислении разрушается
бензольный цикл и образуется 2,3- пиридиндикарбоновая кислота.
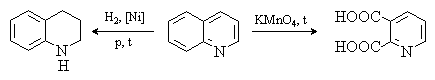
Биологически активные производные хинолина
и изохинолина.
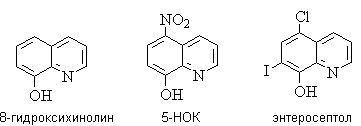
8-Гидроксихинолин и его производные – 8-гидрокси-5-нитрохинолин
(5-НОК) и 8-гидрокси-7-иод-5-хлорхинолин (энтеросептол) – обладают
сильным бактерицидным действием и используются как противовоспалительные и
антисептические средства.
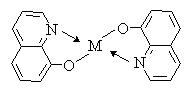
Действие этих препаратов основано на образование
прочных хелатных комплексов с ионами металлов. Таким образом происходит
связывание микроэлементов, необходимых для жизнедеятельности бактерий.
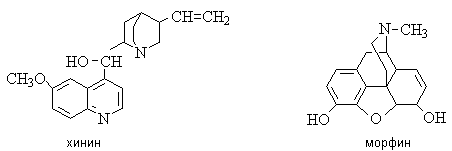
Хинин — алкалоид коры хинного
дерева, эффективное противомалярийное средство.
Алкалоиды опия: морфин — сильнейшее болеутоляющее средство,
наркотик; папаверин — спазмолитическе и сосудорасширяющее средство.
4. Пяти- и шестичленные гетероциклы с
двумя атомами азота.
Имидазол.
Пиразол.
Имидазол и пиразол – 5-членные ароматические гетероциклы, содержащие два
атома азота.
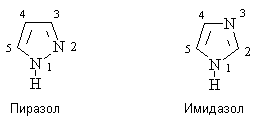
Ароматические системы имидазола и пиразола
включают по 6 p -электронов. При этом один из атомов азота цикла подает в ароматическую
систему один р-электрон (пиридиниевый атом азота), другой атом азота –
неподеленную пару электронов (пиррольный атом азота).
Имидазол и пиразол содержат в молекуле
кислотный центр (связь N-H) и основный центр (пиридиниевый атом азота) и
являются амфотерными соединениями. При этом основные свойства преобладают над
кислотными.
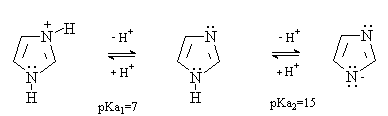
В результате присутствия в молекуле
одновременно кислотного и основного центров имидазол и пиразол ассоциированы
за счет образования межмолекулярных водородных связей.
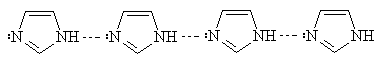
Следствием такой ассоциации являются высокие
температуры кипения и быстрый водородный межмолекулярный обмен между
пиррольным и пиридиниевым атомами азота, который в случае замещенных
гетероциклов приводит к существованию таутомеров.
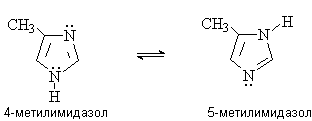
Таутомерные формы быстро превращаются друг в
друга и не могут быть выделены в индивидуальном состоянии.
Особый вид таутомерии характерен для
5-гидроксипиразолов (пиразолонов-5). В растворе они существуют в виде
равновесной смеси гидроки-(I) и оксо-(II,III) таутомерных форм.
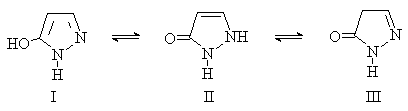
В кристаллическом состоянии наиболее устойчива
форма II.
Биологически активные производные
имидазола и пиразола.
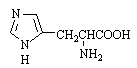
Гистидин — a -аминокислота, входящая в
состав многих белков, в том числе гемоглобина; в составе ферментов
осуществляет кислотный и основной катализ за счет амфотерных свойств
имидазольного цикла.
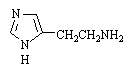
Гистамин – биогенный амин,
продукт декарбоксилирования гистидина; обеспечивает аллергические реакции
организма.
Производные пиразолона-5 — антипирин,
амидопирин, анальгин – ненаркотические анальгетики, жаропонижающие и
противовоспалительные средства.
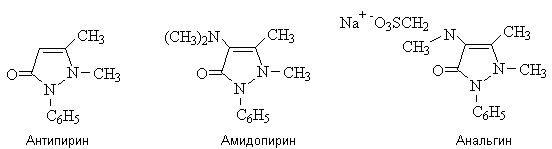
Пиримидин
Пиримидин – 6-членный ароматический гетероцикл с двумя атомами азота.
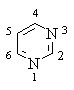
Ароматическая система пиримидина включает 6 p -электронов и
подобна ароматической системе пиридина: каждый атом цикла, в том числе и оба
атома азота, подают в ароматический секстет один р-электрон.
Химические свойства пиримидина подобны
свойствам пиридина. Пиримидин является более слабым основанием, чем пиридин,
за счет электроноакцепторного влияния второго атома азота (![]() =1,3). Снижение, по сравнению с
=1,3). Снижение, по сравнению с
пиридином, электронной плотности на атомах углерода кольца приводит к
инертности пиримидина по отношению к электрофильным реагентам и окислителям.
Реакции нуклеофильного замещении и восстановления в ядре пиримидина, напротив,
протекают легче, чем в пиридине.
Биологически активные производные
пиримидина.
Важную биологическую роль играют гидрокси- и
аминопроизводные пиримидина.
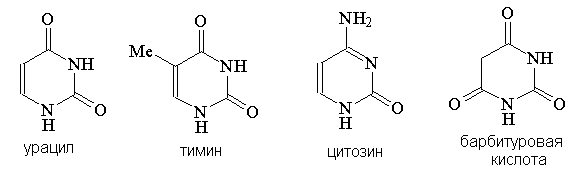
Урацил, тимин и цитозин – нуклеиновые основания; входят в состав нуклеозидов, нуклеотидов,
нуклеиновых кислот. Существуют в таутомерных оксо- и гидроксиформах, переходы
между которыми осуществляются за счет миграции протона между кислородом и
азотом кольца.
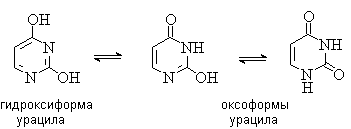
Наиболее стабильными являются оксо-форма для
цитозина и диоксо-формы для урацила и тимина.
Оксо-формы нуклеиновых оснований образуют
прочные межмолекулярные водородные связи.
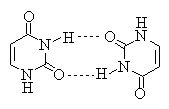
Ассоциация такого типа играет важную роль в
формировании структуры ДНК.
Барбитуровая кислота и ее производные – барбитураты (веронал, люминал) – снотворные и противосудорожные
средства.
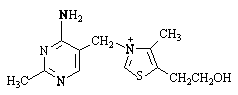
Тиамин (витамин
В1) содержит два гетероцикла –
пиримидин и тиазол.
Тиамин является предшественником кофермента
кокарбоксилазы, принимающего участие в декарбоксилировании a -кетокислот и синтезе
кофермента А.
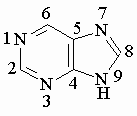
Пурин
Пурин – ароматическое гетероциклическое соединение,
содержащее конденсированные пиримидиновый и имидазольный циклы.
Пурин, подобно имидазолу, существует в виде двух
таутомерных форм. Более стабильной является форма с атомом водорода в положении
7.
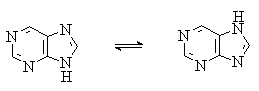
Пурин является амфотерным соединением и образует
соли с сильными кислотами (по атому азота имидазольного цикла) и щелочными
металлами (по NH-группе). При действии алкилирующих реагентов (метилиодид,
диметилсульфат) дает 9-N-алкилпроизводные. Реакции замещения у атомов углерода
ароматического кольца характерны только для замещенных пуринов.
Биологически активные производные
пурина.
Важную биологическую роль играют гидрокси- и
аминопроизводные пурина.
Аденин и гуанин — нуклеиновые основания;
входят в состав нуклеозидов, нуклеотидов, в том числе нуклеотидных коферментов,
нуклеиновых кислот.
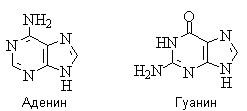
Для аденина известны две таутомерные формы,
являющиеся результатом миграции протона между атомами азота имидазольного цикла.
У гуанина, кроме того, существуют таутомерные гидрокси- и оксоформы.
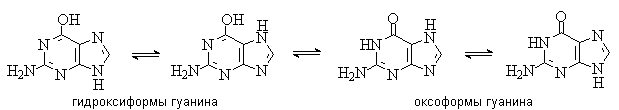
Стабильными таутомерными формами гуанина
являются оксо-формы.
Гидроксипурины – гипоксантин, ксантин,
мочевая кислота – продукты метаболизма пуриновых оснований.
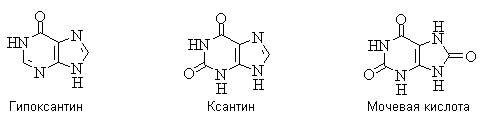
Для них, как и для гуанина, характерны
таутомерные превращения между гидрокси- и оксо-формами. Наиболее стабильными
являются оксо-формы.
Мочевая кислота – конечный продукт метаболизма
пуриновых соединений в организме. Она выделяется с мочой. Соли мочевой кислоты – ураты – откладываются в суставах при подагре, а также в виде почечных
камней.
In vitro аденин и гуанин могут быть превращены
соответственно в гипоксантин и ксантин дезаминированием под действием азотистой
кислоты.
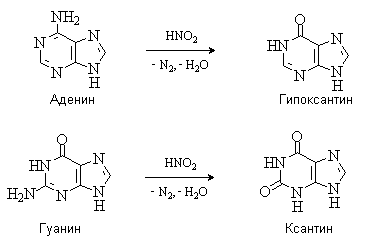
Такие превращения пуриновых оснований в составе
нуклеиновых кислот приводят к мутациям.
Пуриновые алкалоиды – кофеин, теофиллин,
теобромин – метилированные по азоту производные ксантина; содержатся в чае,
кофе, какао-бобах.
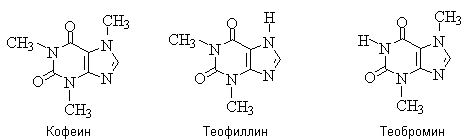
Кофеин – эффективное средство, возбуждающее
центральную нервную систему и стимулирующее работу сердца. Теофиллин и теобромин
менее эффективны, однако обладают сильными мочегонными свойствами.
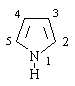
очень интересная лекция)))
а почему нет списка литературы?